KI für nachhaltige Chemie
Die Entwicklung von Arzneimitteln, die nachhaltige Energiespeicherung und die chemische Produktion sind nur einige der Herausforderungen, bei denen die Anwendung von KI in der Chemie neue Wege eröffnen kann. Kjell Jorner, neuer Professor für digitale Chemie am D-CHAB (ICB), möchte diese Entwicklung vorantreiben und im Bereich Katalyse den Übergang zu einer nachhaltigen chemischen Produktion beschleunigen.
Kjell Jorner ist analog unterwegs, wenn er abseits des Büros über digitale Lösungen nachdenkt: Der gebürtige Schwede ist passionierter Läufer, angehender Raclette-Enthusiast und als Kaffeegourmet Besitzer "zu vieler" Kaffeemaschinen, wie er findet, inklusive Bialetti (sein präferiertes Modell). Auch am Tag des Interviews offeriert er Kaffee in den Räumen, die Büro und virtuelles Labor zugleich sind. Von hier aus erforschen Kjell Jorner und sein Team die molekulare Welt mit Hilfe künstlicher Intelligenz, die selbst erstmal sowohl Daten als auch Wissen benötigt, um Antworten liefern zu können. Künstliche Intelligenz als geduldiger Schüler und – so die Hoffnung – Teil der (chemischen) Lösung für drängende Probleme.

Computergestützte Forschung bietet sich für Forschungsfragen an, die im Labor nur schwer oder gar nicht untersucht werden können: Vorhersagen für Dinge beispielsweise, die experimentell unmöglich oder zu teuer und zeitaufwendig wären. „Entdeckungen zu beschleunigen ist ein Hauptzweck von computergestützten Methoden bzw. künstlicher Intelligenz“, sagt Jorner, «so lässt sich etwa die Zeit von der Identifizierung eines Zielmoleküls bis zur Markteinführung eines Medikaments signifikant verkürzen. Ähnlich verhält es sich im Bereich Reaktivität und Katalyse, mein Spezialgebiet. Mit den Methoden, die wir entwickeln, könnte KI künftig helfen, neue Katalysatoren viel schneller zu finden.»
Wenn der Lernstoff fehlt
Ursprünglich hatte sich Jorner in Uppsala auf physikalisch-organische Chemie fokussiert und erforschte als Doktorand die Photochemie organischer Verbindungen. «Ich bin aber bald in die Simulation abgedriftet. Die Arbeit am PC machte mir Spass und es gefiel mir, schnelle Ergebnisse zu erzielen. Indem man Tests via Simulationen macht, erspart man sich die Synthese von Molekülen, die am Ende nicht die gewünschten Eigenschaften aufweisen. Man kann sich auf die vielversprechenden konzentrieren.»
Das klingt einfacher als es ist. In der Chemie sind Modellierungen, speziell mit Hilfe von künstlicher Intelligenz (KI), eine grosse Herausforderung. Dazu muss man wissen: KI ist ein vielschichtiger Oberbegriff. Es gibt dabei Expertensysteme (z.B. mechanistische Modelle, basierend auf chemischen Theorien), die zwar intelligent sind, aber nicht von Daten lernen, sondern Vorhersagen nach vorgegebenen Regeln treffen, und es gibt das heute dominierende Maschinelle Lernen (ML), wo das System mit möglichst vielen Daten trainiert wird, daraus lernt und auf dieser Basis selbst Regeln für Vorhersagen aufstellt (z.B. für chemische Reaktionen). Teil des ML ist auch das Deep Learning – ein künstliches neuronales Netz mit Eingabe, Ausgabe und vielen versteckten Schichten dazwischen.
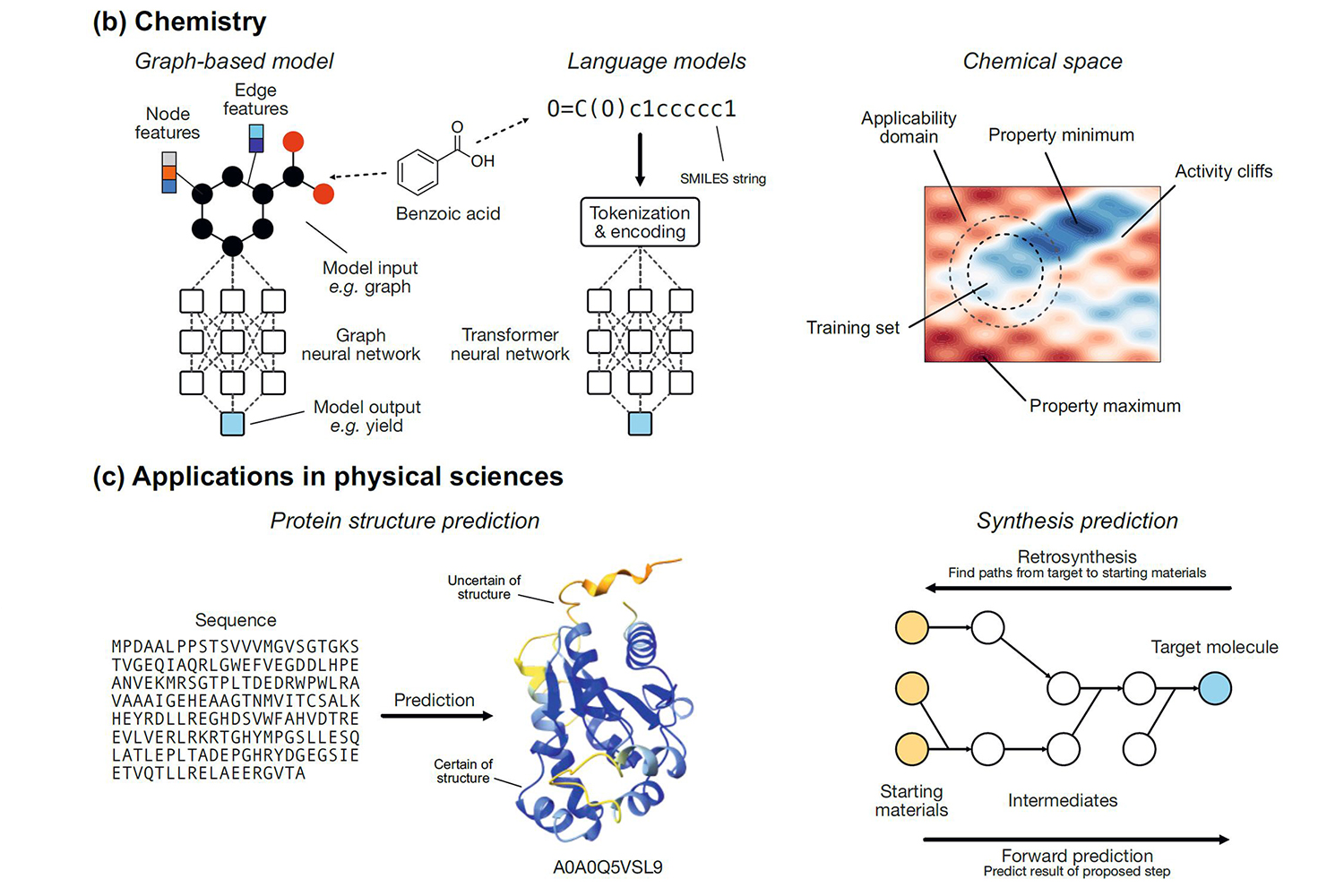
Für eine optimale Perfomance müssen ML-Systeme mit einer möglichst grossen Datenmenge trainiert werden. In der Chemie ist diese aber nur für wenige Bereiche verfügbar – z.B. für Retrosynthesemodelle (trainiert mit ca. 3,3 Mio. Reaktionen) – und selbst dort sind die Datensätze um Welten kleiner als jene der Bildsysteme (DALL-E: ca. 250 Mio. Bild-Text-Paare) oder Sprachsysteme (ChatGPT 3.5: ca. 500 Mrd. Token). «Ein Problem in der Chemie ist, dass die Daten meist nicht im richtigen Format zugänglich sind», betont Jorner. «Auch bei der Datenqualität gibt es zwangsläufig Unterschiede zwischen den Forschungsfeldern». All das erschwert die Modellierung.
Wie man aus wenig Daten viel herausholt
Daher versucht man die Datensätze durch spezielle Methoden mit Daten anzureichern, um dem Computer eine bessere Vorstellung zu geben. «Will man ihm beibringen, wie ein Molekül beschaffen ist, kann man dies zum Beispiel durch Deskriptoren tun: Zahlenwerte, die die Eigenschaften des Moleküls beschreiben, z.B. Ionisierungspotenzial, Elektronenaffinität etc.», erklärt Jorner. «Deskriptoren kann nicht jeder erstellen, es ist Fachwissen nötig. Deshalb gibt es für wichtige Molekülgruppen bereits Kataloge. Ich selbst war an einem Katalog für Phosphin-Liganden beteiligt, welche für die Katalyse eine wichtige Rolle spielen.»

Auch Hybridmodelle, die physikalische Simulationen mit Maschinellem Lernen kombinieren, können helfen eine brauchbare Genauigkeit trotz geringer Datenmenge zu erzielen. Diesen Weg verfolgte Kjell Jorner 2018 als Postdoktorand bei AstraZeneca in Grossbritannien. «Um ein Molekül für ein Medikament herzustellen, muss man das Molekül schrittweise aufbauen. Unsere Aufgabe war es Berechnungswerkzeuge zu entwickeln, die vorhersagen können, ob die Schritte erfolgreich sein würden und ob sie selektiv genug wären, damit ein sauberes Produkt entsteht und nicht eine Mischung, die man kostspielig wieder aufreinigen müsste,» schildert er das Projekt.
Jorner und seine Kollegen versuchten es mit einem hybriden Ansatz (Jorner et al 2021) und wählten die nukleophile aromatische Substitutionsreaktion als Anwendungsziel: «Wir haben die Schritte der chemischen Reaktion mit einem mechanistischen Simulationsmodell abgebildet und dieses Modell mithilfe von KI mit Deskriptoren ergänzt, um eine höhere Genauigkeit bei der Vorhersage zu erzielen». Die Idee erwies sich als erfolgreich: Das Modell wurde am Ende von AstraZeneca und auch von anderen Pharmaunternehmen wie Pfizer eingeführt.
Nachhaltige chemische Produktion durch KI
2021 ging Jorner an die Universität von Toronto und erforschte dort das molekulare Design von Katalysatoren und organischen elektronischen Materialien – Wissen, das ihm nun als Assistenzprofessor für Digitale Chemie am Institut für Chemie und Bioengineering am D-CHAB der ETH zupasskommt. Hier wird er im Rahmen des D-CHAB assoziierten NCCR Catalysis mit seiner Gruppe an digitalen Werkzeugen forschen, die die Entdeckung neuer Katalysatoren beschleunigen, bestehende Katalysatoren verbessern und Versuchsbedingungen optimieren. Dies soll z.B. dazu beitragen Ersatz für fossile Brennstoffe als Ausgangsmaterial für die chemische Produktion zu finden, nachhaltigere Methoden für die Arbeit mit Feinchemikalien zu entwickeln oder die Herstellung von Chemikalien aus Biomasse zu ermöglichen.
Zudem plant er ein Wahlfach zur Digitalen Chemie und freut sich auf die Betreuung der Studierenden. Seine Gruppe wächst und zudem stehen der Hochschule spannende Zeiten bevor. «An der ETH diskutieren Forschende, Lehrende und Führungskräfte derzeit intensiv über den Einsatz von KI-Werkzeugen . Alles verändert sich so schnell, und die Menschen haben Mühe, damit Schritt zu halten. Da ein Verbot von KI aber nicht durchführbar zu sein scheint", meint Jorner, "sollten wir unsere Studierenden mit dem Wissen ausstatten, wie man diese Werkzeuge richtig einsetzt, denn diese Fähigkeiten werden auf dem Arbeitsmarkt unverzichtbar sein. Der breite Einsatz von KI macht es jedoch erforderlich, dass wir unsere Lehr- und Bewertungsmethoden anpassen".

Insgesamt seien die Folgen dieser Entwicklungen aber schwer abzuschätzen, räumt Jorner ein, «prominente Stimmen fordern daher einen Stopp der KI-Forschung. Die Entwicklung wird sich jedoch kaum aufhalten lassen. Ich teile die Ansicht des ETH AI Centers, dass es besser ist, die akademische Forschung offen und transparent weiterzuführen. Andere werden es auch tun und wir würden sonst nur Transparenz einbüssen.»
In der Tat birgt KI grosses Potenzial. «Unsere Vision wäre ein System, welches auf Anfrage hin Katalysatoren mit geeigneten Eigenschaften designen kann. Dann könnte man sie direkt testen und synthetisieren.» Etwa in einem vollautomatischen Labor? «Möglicherweise, dahin wird die Entwicklung gehen», vermutet der Professor. Prototypen gibt es bereits. Doch kein Grund zur voreiligen Aufregung. Bis zu einer Implementierung wird, wie es klingt, wohl noch sehr viel Kaffee durch die Espressomaschinen dieser Welt fliessen, auch durch Kjell Jorners Moka-Pot.

Weiterführende Information
Jorner K, Brinck T., Norrby PO, Buttar D (2021): Machine learning meets mechanistic modelling for accurate prediction of experimental activation energies. Chem. Sci., 2021, 12, 1163. DOI: externe Seite https://doi.org/10.1039/D0SC04896H
Jorner K (2023): Putting Chemical Knowledge to Work in Machine Learning for Reactivity. Chimia 2023, 77, 22, DOI: externe Seite 10.2533/chimia.2023.22.