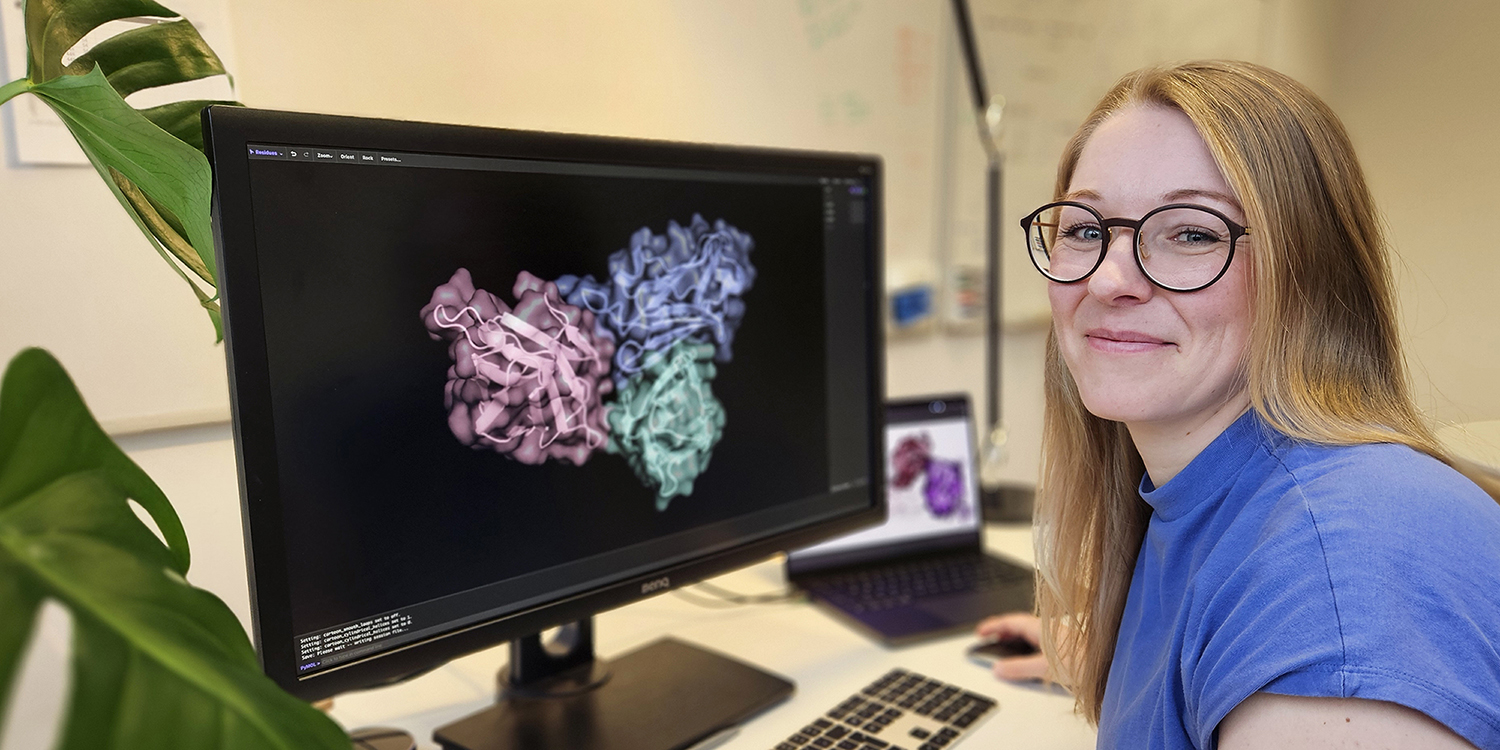
Peptid-basierte Wirkstoffe ohne Grenzen
Peptide fungieren im Körper als Signalvermittler und sind auch als Therapeutika im Aufschwung. Noch ist ihre Wirksamkeit aber oft durch schnellen Abbau und Ausscheidung limitiert. Nathalie Grob, neue SNF-Assistenzprofessorin für Peptid-basierte Wirkstoffentdeckung, erforscht Methoden, um diese Limitierung zu umgehen und konzentriert sich auf bisher wenig untersuchte oder schlecht therapierbare Krankheiten, die Frauen und Mädchen betreffen.
Nathalie Grob hat ein „Pensionisten-Hobby“, wie sie es augenzwinkernd nennt. Die Schweizerin ist passionierte Vogelbeobachterin – ob nun beim Wandern, Langlaufen oder kurz zwischen den Meetings vom Bürofenster aus. Dort ziehen Milane, Habichte und Krähen ihre Kreise. Vogelbeobachtung sei die perfekte Freizeittätigkeit zum Entspannen, schwärmt die neue Assistenzprofessorin für Peptid-basierte Wirkstoffentdeckung am DCHAB, vor allem, wenn es in Lehre und Forschung mal turbulent zugeht.

In der Tat sind Peptid-basierte Wirkstoffe derzeit in aller Munde – unter anderem wegen der GLP1 Rezeptor-Agonisten, welche als Mittel für Diabetes und Gewichtsverlust Furore machen, ja sogar auf Social Media trenden. Das Beispiel illustriert, wie gross der Markt ist und wie vielfältig Peptide – kurze Aminosäureketten mit speziellen Eigenschaften – als Arzneimittel agieren können. Sie sind auch oft selektiver und potenter als die viel verwendeten Small Molecules (niedermolekulare Verbindungen mit geringer Grösse) und haben daher weniger Nebenwirkungen.
Nathalie Grob hat sich ebenfalls auf therapeutische Peptide spezialisiert, obgleich nicht auf das genannte Beispiel. Die Assistenzprofessorin will neue Strategien zur Entdeckung von Peptidarzneimitteln entwickeln. Denn trotz vorteilhafter Eigenschaften gibt es bei Peptid-basierten Wirkstoffen immer noch Hindernisse. Dafür möchte Nathalie Grob mit ihrer Gruppe Lösungen finden und Therapieoptionen für schlecht behandelbare Krankheiten schaffen, die vorwiegend Frauen betreffen – ein persönliches Anliegen der Pharmazeutin, die sich bereits als Studentin und Mitglied bei der Vereinigung WiNS sehr für Frauenbelange einsetzte.

Ihre Begeisterung für Peptide entwickelte Nathalie Grob während ihrer Masterarbeit an der Universität Uppsala in Schweden. Dort synthetisierte die Pharmazeutin Varianten von Kalata B7, einem komplex verknoteten Peptid aus einer Pflanze, die in Zentralafrika bei der Geburtshilfe eingesetzt wird.
Während ihres Doktorats an der ETH Zürich beschloss sie auch künftig in der Peptidchemie zu bleiben: „Bis heute finde ich es faszinierend, dass unser Körper nur 20 Aminosäuren benötigt, um Peptide und Proteine herzustellen, die alle wichtigen Körperfunktionen regulieren. Es ist, als hätte man Legosteine in 20 Formen, aus denen sich je nach Reihenfolge z.B. ein Helikopter oder ein Traumhaus erschaffen lassen. Als Peptidchemikerin hat man in der Hand, wie man die Moleküle zusammensetzt und kann sogar über die 20 Aminosäuren hinausgehen. Das ist ein schönes Gefühl,“ zeigt sich Grob begeistert.
Alleskönner mit Grenzen
Im Körper verrichten Peptide viele wichtige Aufgaben. Beispielsweise modulieren sie Protein-Protein-Interaktionen – ein gutes therapeutisches Angriffsziel, da diese wichtige Zellfunktionen regulieren und somit relevante Stellschrauben für viele Erkrankungen wie Krebs darstellen. Möchte man Peptide therapeutisch einsetzen, um an diesen Stellschrauben zu drehen, stösst man aber auf ein evolutionsbiologisches Problem.
„Peptide werden normalerweise schnell abgebaut“, erklärt Grob. „Das ergibt Sinn, denn viele natürliche Peptide sind Hormone. Diese müssen zwecks Regulation schnell ein- und ausgeschaltet werden können, etwa durch enzymatische Scheren. Zudem werden Peptide leicht über die Nieren ausgeschieden und bleiben oft nicht lang genug im Körper, um als Arzneistoff zu wirken.“
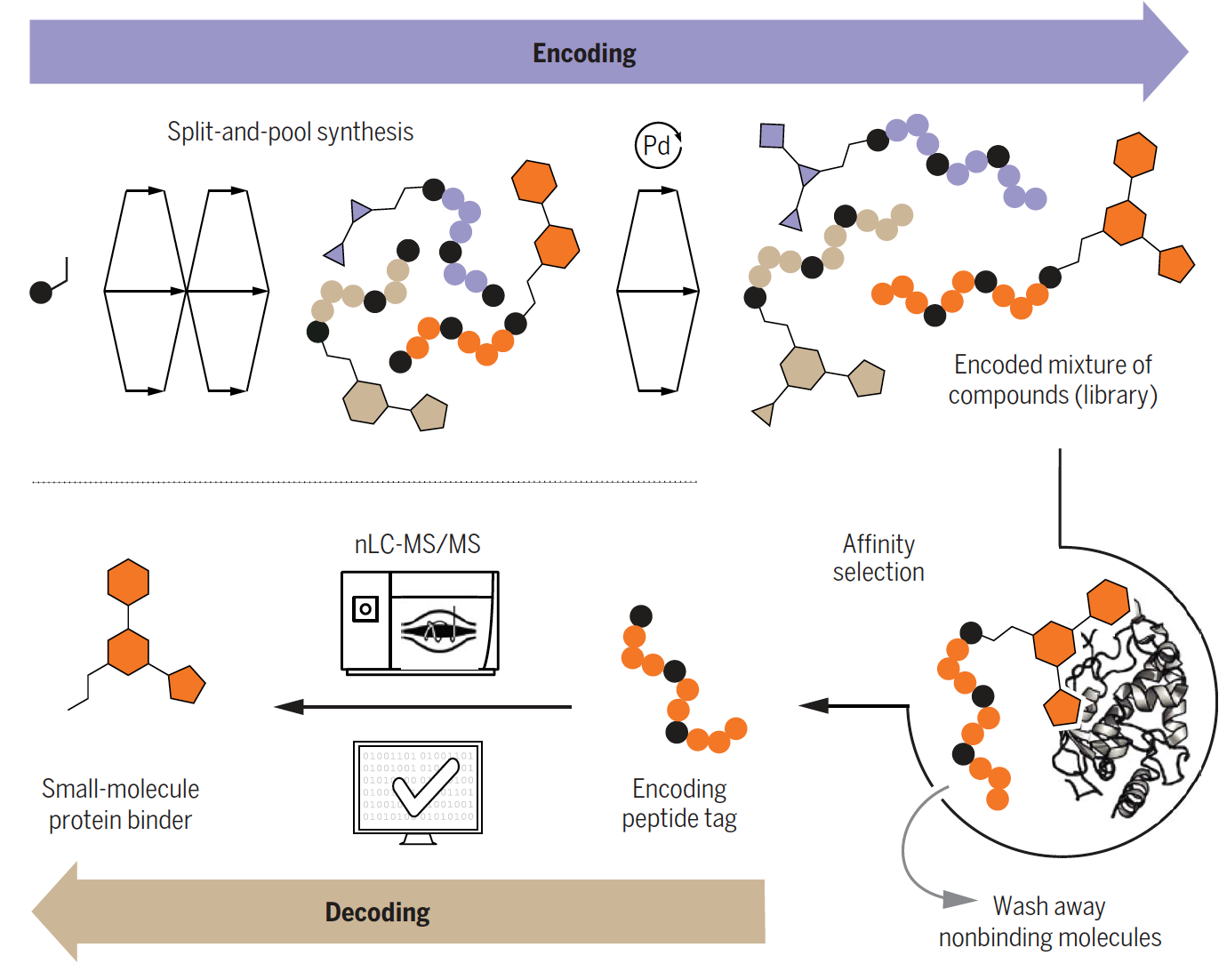
Peptide als Barcodes
Die Kurzlebigkeit der Peptide ist einer der Gründe, weshalb ein Grossteil der heutigen Medikamente auf Small Molecules basiert. Als Postdoc am MIT arbeiteten Nathalie Grob und ihr Kollege Simon Rössler daher zunächst an der Idee, Peptide als Hilfsmittel für die Suche nach Small Molecules einzusetzen (Rössler et al 2023).
„In der Wirkstoffentdeckung verwendet man häufig Small Molecule-Bibliotheken: zehntausende archivierte Verbindungen, deren Affinität zu einem bestimmten Protein geprüft wird. Um eine Verbindung unter Tausenden durch eine affinitätsbasierte Selektion identifizieren zu können, braucht sie aber eine Markierung“, erklärt Grob. „Wir haben während des Lockdowns einen Peptid-basierten Barcode entwickelt . Die angehängten künstlichen Peptide können durch eine gängige Software schnell ausgelesen werden und ermöglichen so die Identifikation.“
So weit, so nützlich. Doch Protein-Protein Interaktionen, die molekular gesehen oft riesige Kontaktflächen bilden, kann man nur schwer mit Small Molecules beeinflussen, sprich je nach Krankheitsbild inhibieren oder stabilisieren. Hier wären grössere Peptid-basierte Arzneistoffe besser geeignet. Das brachte Nathalie Grob – nunmehr zurück aus dem lockdownbedingt ungemütlichen Homeoffice – zur zentralen Frage, wie sich der erwähnte Abbau und die Ausscheidung verhindern lassen könnten.
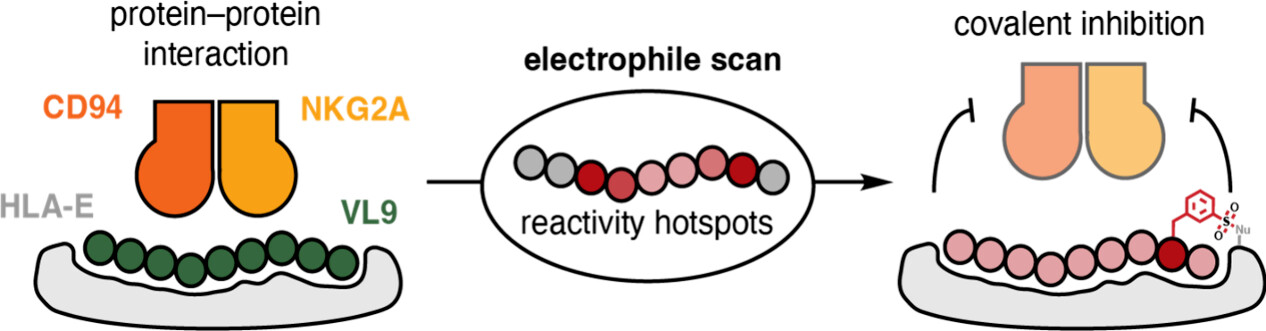
Peptide als Arzneimittel
Unter Grobs Leitung entwickelten Forschende am MIT und Industriepartner in San Francisco die Strategie des „elektrophilen Scannings“ (Grob et al 2024): „Um eine vorschnelle Ausscheidung zu verhindern, muss der Peptid-basierte Wirkstoff stärker am Zielprotein verankert werden. Dies lässt sich z.B. durch kovalente Bindungen bewerkstelligen“, erläutert Grob. „Wir haben ein Werkzeug etabliert, mit dem wir reaktive Bindungsstellen schnell finden und entsprechende Peptid-Binder mit elektrophilen Gruppen bauen können. Diese verankern den Peptid-basierten Wirkstoff am Zielprotein. Im Versuch konnte das eingesetzte Peptid die angestrebte Protein-Protein Interaktion so erfolgreich inhibieren.“
Vor einem enzymatischen Abbau schützt diese Methode allerdings nur bedingt. Diesen Schritt will Nathalie Grob nun an der ETH Zürich angehen. Dort wird sie dank SNF-Starting Grant eine unabhängige Forschungsgruppe aufbauen und neue künstliche Peptide mit verbesserten Eigenschaften entwickeln: „Wir hoffen so Wirkstoffe zu erhalten, welche nicht so schnell von enzymatischen „Scheren“ im Körper erkannt und abgebaut werden.“
Im Fokus möglicher Anwendungsbereiche stünden dabei schlecht therapierbare oder unzureichend erforschte Krankheiten, die vorwiegend Frauen und Mädchen betreffen.

«Rund zehn Prozent der Frauen leiden zum Beispiel unter Endometriose, einer äusserst schmerzhaften Erkrankung, bei der Gebärmutterschleimhautzellen ausserhalb der Gebärmutter wachsen. Trotz der vielen Betroffenen wurden bislang erstaunlich wenig Mittel zur gezielten Diagnostik und Therapie entwickelt. Peptid-basierte Wirkstoffe könnten Teil der Lösung sein. Wir hoffen, mit unserer Forschung einen wertvollen Beitrag zu leisten.»Prof. Nathalie Grob
Mittlerweile hält Nathalie Grob auch ihre ersten Vorlesungen an der ETH und freut sich auf die Zusammenarbeit mit den Studierenden: „Ich möchte sie dabei unterstützen, ihre individuellen Stärken zu erkennen und weiterzuentwickeln.“ Neben der Vermittlung fachlicher Expertise lege sie auch grossen Wert auf die Förderung von Schlüsselkompetenzen wie kritischem und interdisziplinärem Denken, Teamarbeit und die Kommunikation komplexer Zusammenhänge. „Mir ist wichtig, dass die Studierenden nicht nur Wissen erwerben, sondern auch lernen, wie sie dieses anwenden können, um ihre eigenen Interessen und Karriereziele zu verfolgen.“

Nathalie Grob erlangte ihre Abschlüsse in Pharmazeutischen Wissenschaften und Pharmazie an der Universität Basel. Für ihre MSc-Arbeit schloss sie sich der Gruppe von Prof. Ulf Göransson an der Universität Uppsala in Schweden an und promovierte schliesslich an der ETH Zürich bei Prof. Roger Schibli und Prof. Thomas Mindt, wo sie an der Entwicklung von radioaktiv markierten Peptiden für die Diagnose und Behandlung bestimmter Krebsformen arbeitete. Von 2020 bis 2023 war Nathalie Grob Postdoktorandin bei Prof. Bradley Pentelute am Massachusetts Institute of Technology in Cambridge,USA. Ihre Forschung konzentrierte sich auf die Entdeckung neuer Wirkstoffe in Form von niedermolekularen Molekülen und Peptiden. 2024 kehrte Grob, unterstützt durch einen Starting Grant des Schweizerischen Nationalfonds, als Assistenzprofessorin ans D-CHAB zurück, um die Forschungsgruppe "Peptid-basierte Wirkstoffentdeckung" zu gründen.
Save the date
Prof. Nathalie Grobs Einführungsvorlesung findet am 3. April 2025 im Audimax (ETH Gauptgebäude) statt. Weitere Informationen folgen.
Weitere Informationen
Rössler SL, Grob NM, Buchwald SL, Pentelute BL (2023): Abiotic peptides as carriers of information for the encoding of small-molecule library synthesis. Science 2023. Vol 379, Issue 6635 pp. 939-94. externe Seite DOI: 10.1126/science.adf1354
Grob NM, Remarcik C, Rössler SL, Wong JYK, Wang JCK, Tao J, Smith CL, Loas A, Buchwald SL, Eaton DL, López MP, Pentelute BL (2024): Electrophile Scanning Reveals Reactivity Hotspots for the Design of Covalent Peptide Binders. ACS Chemical Biology 2024 19 (1), 101-109 . externe Seite DOI: 10.1021/acschembio.3c00538